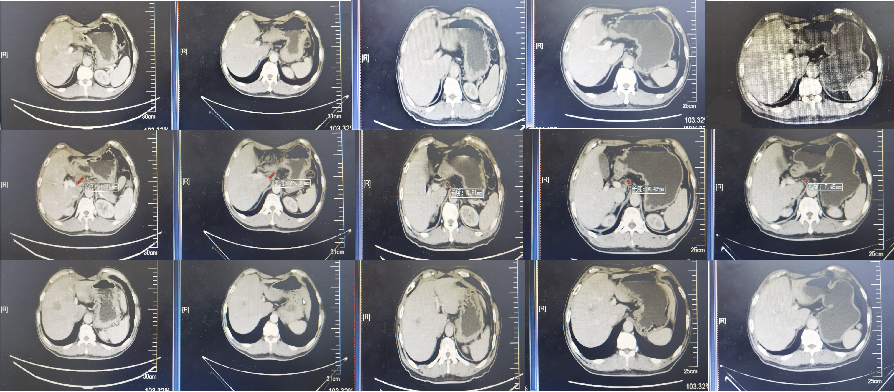
根据世界卫生组织统计,截止至2020年,胃癌在全球癌症发病率和死亡率中分别位居第六位和第四位[1]。我国胃癌高发,且较多的患者就诊是已处于晚期,严重影响患者的生存预后[2]。对于这部分患者,一线治疗策略能否起效,成为能否延长患者生存,改善预后的关键。近年来随着以程序性死亡受体-1/程序性死亡受体-配体1(PD-1/PD-L1)单抗为代表的免疫治疗的兴起,国产PD-1单抗替雷利珠单抗联合化疗的疗效已在晚期胃癌一线治疗实际中得到验证,在转化治疗中也表现出色。 本期百启新生分享一例HER2阴性晚期胃腺癌伴肝转移的老年病例,患者在经过免疫联合化疗一线治疗8周期后,疗效达到部分缓解(PR),病灶改善并最终行手术切除,术后病理达到病理完全缓解(pCR),获得了生的希望。 (病例点评专家:郑志超主任医师;病例分享专家:刘勇主任医师) 郑志超 教授 辽宁省肿瘤医院胃外科主任、主任医师 医学博士 硕士研究生导师(中国医科大学、大连医科大学、大连理工大学) 辽宁省抗癌协会胃癌专业委员会候任主任委员 辽宁省医学会外科分会胃肠学组组长 辽宁省抗癌协会肿瘤营养与支持治疗专业委员会主任委员 中国抗癌协会第六届胃癌专业委员会常委 中国抗癌协会第一届肿瘤营养专业委员会委员 中国抗癌协会胃肠道间质瘤诊疗专业委员会常委 中国医师协会外科医师分会胃肠道间质瘤诊疗专业委员会常委 辽宁省医师协会外科医师分会第一届委员会常委 沈阳市医师协会普外科分会副主任委员 中国医药教育协会腹部肿瘤专业委员会辽宁省培训基地副主任委员 中国医药教育协会腹部肿瘤分会常委 刘勇 教授 辽宁省肿瘤医院胃外一科主任医师 辽宁省医学会外科学分会第九届委员会胃肠外科学组组员兼秘书 辽宁省医学会肠外肠内营养学分会第六届委员会青年委员会委员 辽宁省医学会肠外肠内营养学分会第六届委员会肿瘤营养学组组员 辽宁省抗癌协会营养与支持治疗委员会第二届委员会秘书 辽宁省营养学会第六届临床营养专业委员会委员 东北三省肠外肠内营养支持专业委员会第五届委员会委员 辽宁省营养学会体重管理分会委员 世界华人医师协会会员 病例基本资料 一般资料:男性,67岁 主诉:上腹部胀痛3个月 现病史:患者3个月前出现上腹部胀痛不适,以餐后为重。伴有食欲减退,反酸、嗳气,恶心、无呕吐,进食量明显减少。无呕血,偶有黑便。曾口服奥美拉唑,症状无缓解。近半月症状加重,就诊于当地医院行胃镜检查,诊断为“胃癌”。为求进一步治疗而来我院。患者病来食欲差,饮食差,二便不规律。3个月来体重下降5公斤。 既往史:糖尿病史20年,口服阿卡波糖治疗;吸烟史40年,每天5支;饮酒史40年,每日2两。 家族史:舅舅患肺癌、姑姑患脑胶质瘤,均病逝。 体格检查:身高:165cm ,体重:57kg ,体表面积(BSA):1.655㎡ ,体质指数(BMI):20.95kg/㎡ 一般情况可,无明显异常体征,Karnofsky功能状态(KPS)评分:90分,营养状态评估:NRS2002评分 3分;患者主观整体评估(PG-SGA)评分 7分 辅助检查: 胃镜:胃窦变形,见巨大不规则隆起,表面凸凹不平,局部见暗红色血痂,质脆易出血。病变处管腔严重变形狭窄,幽门口未见,内镜不能通过。 病理诊断:胃窦:腺癌(中低分化),C-erbB-2(0),CPS评分(15);MLH1(+),MSH2(+), MSH6(+),PMS2(+); 2022.1超声胃镜:胃窦占位浸透浆膜层,伴胃周淋巴结增大,胰腺颈部增大半低回声改变,腹膜后低回声团块 2022.1 肝脏增强MRI:肝S8段肿物,考虑恶性,倾向转移瘤,不完全除外胆道原发肿瘤;胃窦胃壁增厚,符合胃癌,胰颈部上方多发肿大淋巴结,考虑转移。 2022.1 血常规:白细胞5.03 *10^9/L ;血红蛋白浓度113g/L ↓;红细胞3.34 *10^12/L ↓; 2022.1 生化:肝功:白蛋白 35.9g/L ↓;ALT 16U/L;肾功:正常 2022.1 肿瘤标记物:CA72-4:8.79U/mL↑;CA19-9:160.8U/mL↑;CEA:38.84ng/mL↑;CA12-5:111.4U/ml↑; 诊断:胃癌(cStage: T4aN+M1 Ⅳ期)、肝转移、中度营养不良 治疗经过 术前治疗阶段 结合患者病史及实验室检查结果,经多学科会诊(MDT)讨论后完善肝脏穿刺,考虑胃腺癌伴肝转移,免疫组化结果提示HER2(-)、MSS、CPS(15)。根据《NCCN指南(2022版)》及《CSCO胃癌诊疗指南推荐(2022版)》[3-4],予PD-1单抗 + XELOX(替雷利珠单抗3mg/kg d1+奥沙利铂130mg/m2 d1+卡培他滨1000mg/m2 d1-d14 bid)方案治疗,定期评估影像学、血常规及肿瘤标志物等指标。治疗4周期后行MDT讨论:患者化疗一周期后自觉进食好转,两周期后进食正常,偶有I度胃肠道反应,轻度末梢神经炎,无骨髓抑制出现,耐受良好,结合影像学及肿瘤标志物结果,疗效判定:PR。故继续行转化治疗。予当前方案4周期后再次行MDT讨论:患者化疗8周期偶有I度胃肠道反应,II度末梢神经炎,无骨髓抑制,耐受良好,继续检测影像学及肿瘤标志物指标,疗效判定:PR。由于患者MR检查提示肝转移灶已经模糊不清,术前治疗已长达7个月,持续处于PR状态,病情控制良好。因此考虑手术治疗+肝转移灶术中探查,可行切成或射频治疗。 辅助检查: 影像学: 患者CT影像学变化[入院时(2022.1)vs治疗2周期时(2022.3)vs治疗4周期时(2022.5)vs治疗6周期时(2022.6)vs治疗8周期时(2022.8)] 患者MRI影像学变化[入院时(2022.1)vs治疗8周期时(2022.8)] 血检: 2022.5.9血常规:白细胞6.20 *10^9/L ;血红蛋白浓度102g/L ↓ ;红细胞3.13 *10^12/L ↓; 2022.5.9血生化:肝功:白蛋白 41.5g/L;ALT 24U/L;肾功:正常; 2022.8.15血常规:白细胞5.11 *10^9/L;血红蛋白浓度118g/L↓;红细胞3.71 *10^12/L↓; 2022.8.15血生化:肝功:白蛋白 42.9g/L;ALT 30U/L;肾功:正常; 肿瘤标志物: 2022.5.9肿瘤标志物:CA72-4:11U/mL↑、CA19-9:7.31U/mL↑、CEA :4.68ng/mL↑、CA12-5:8.5U/ml↑; 2022.8.15肿瘤标志物:CA72-4:0.69U/mL↑,CA19-9:10.49U/mL↑,CEA :5.64ng/mL↑,CA12-5:44.1U/ml↑; 手术治疗及术后治疗阶段: 患者于2022-8-24行根治性远端胃大部切除术+结肠前BillrothⅡ吻合+远端空肠行布朗吻合+淋巴结D2清除术,术中见肿瘤位于胃窦近幽门处,环周4/4。已浸润浆膜层,浆膜分型:反应型。术中探查盆腔腹腔肝脏未出现转移,并请肝胆科术中会诊,行术中超声检查,仍未查到肝脏转移灶。术后患者恢复良好,第6天拔管拆线,各项检验结果正常,肿瘤标志物下降至正常水平,于第7天痊愈出院。术后病理提示:胃:符合慢性炎症伴上皮增生,未见确切癌组织。病理肿瘤退缩分级(TRG):1级,pCR。目前术后治疗:免疫+化疗(单药口服)治疗中。 患者肿瘤标志物变化[入院时至术后第一次化疗(2022-9)] 病例总结 本例患者为老年男性,诊断为晚期胃癌(cStage: T4aN+M1 Ⅳ期)、肝转移、中度营养不良。免疫组化结果提示Her2(-)、MSS、CPS(15)。根据NCCN及CSCO指南建议,予PD-1单抗 + XELOX(替雷利珠单抗3mg/kg d1+奥沙利铂130mg/m2 d1+卡培他滨1000mg/m2 d1-d14 bid)方案治疗8周期,疗效评估PR,病灶较前明显好转。转化治疗成功后行手术治疗,术后恢复良好,术后病理达到pCR,目前继续免疫+化疗(单药口服)治疗中。 专家点评 晚期胃癌患者转移比例高、常伴营养不良,治疗耐受性差,因此一线治疗方案选择尤为关键。既往一线化疗治疗以化疗为主,中位总生存期(OS)不超过1年[5]。HER2阴性的胃癌占胃癌的大多数,目前HER2阴性胃癌一线治疗仍以化疗为主,但近年来以PD-1/PD-L1单抗为代表的免疫治疗的兴起,也给患者带来了新的希望。 CheckMate 649研究是一项全球多中心,开放标签,Ⅲ期临床研究,是目前全球针对晚期胃癌一线治疗开展的入组病例最多的多中心临床研究,奠定了化疗基础上联合PD-L1单抗在晚期HER2阴性且联合阳性分数(CPS)>5胃癌患者一线治疗中的地位。在CheckMate 649研究已公布的中国患者亚组更新数据中,在PD-L1 CPS≥5和PD-L1 CPS≥1的患者以及PD-L1单抗+化疗vs.化疗的所有随机化患者中,均观察到有临床意义的OS和无进展生存期(PFS)改善,与全球研究人群一致[6]。基于这一结果,《CSCO胃癌诊疗指南(2022年版)》中对于晚期HER2阴性患者,推荐PD-1联合化疗的基本方案[4]。 替雷利珠单抗是我国自主研发的PD-1单抗,在晚期胃癌治疗领域表现出色。RATIONALE 205研究显示[7],替雷利珠单抗联合化疗一线治疗胃癌/胃食管结合部腺癌(GC/GEJ),其总人群的客观缓解率(ORR)达46.7%,疾病控制率(DCR)为80%,达到缓解的中位时间为9.3周。中位无进展生存期(mPFS)达6.1个月,15.4个月的中位随访期内中位OS未达到,取得了显著疗效与持久获益。后续探索替雷利珠单抗联合化疗的全球多中心III期临床研究RATIONALE 305研究的中期结果提示,相较于安慰剂联合化疗,替雷利珠单抗联合化疗一线治疗局部晚期不可切除或转移性GC/GEJ患者,可为PD-L1表达人群带来显著生存获益,进一步彰显替雷利珠单抗的实力。此外,围手术期免疫治疗方面,替雷利珠单抗联合化疗同样表现不俗。近日登陆Frontiers in Oncology杂志的WuhanUHGI001研究也显示,替雷利珠单抗联合SOX方案用于进展期GC/GEJ新辅助治疗的pCR率达到25%,主要病理缓解(MPR)率达到53.1%。提示免疫联合治疗在GC/GEJ的新辅助治疗和转化治疗中可能具有良好的应用前景[8]。 结合本病例,老年男性患者,就诊时已处于疾病晚期,且伴肝转移,根据免疫组化结果考虑免疫治疗指征明确,故予替雷利珠单抗联合化疗4周期,疗效评估为PR,有效改善病灶,提示转化治疗可行性,且于8周期后再次评估为PR,并成功行手术切除,术后病理结果令人满意。本病例显示了在化疗基础上联合替雷利珠单抗免疫疗法在晚期胃癌一线治疗的可靠疗效。期待更多的临床研究证据支持,以寻求更进一步的突破! 参考文献: [1] https://gco.iarc.fr/today/online-analysis-multi-bars?type_multiple=%257B%2522inc%2522%253Atrue%252C%2522mort%2522%253Atrue%252C%2522prev%2522%253Afalse%257D [2] 左婷婷, 郑荣寿, 曾红梅,等. 中国肿瘤临床, 2017, 44(1):52-58. [3] National Comprehensive Cancer Network. (NCCN) Clinical Practice Guidelines in Oncology. Gastric Cancer, Version 2. 2022. [4] 中国临床肿瘤学会指南工作委员会. 北京:人民卫生出版社,2022. [5] Bang Y J, et al. The Lancet, 2010, 376(9742): 687-697. [6] Shen, L. et. al. 2021,AACR 2021, presentation number CT184, April 2021. [7] Xu J, et al. Clin Cancer Res . 2020 Jun 19;clincanres.3561.2019. [8] Yin Y, et al. Front Oncol. 2022 Aug 30;12:959295.